搜索结果: 1-15 共查到“生物学 核小体”相关记录56条 . 查询时间(0.332 秒)

2023年9月15日,中国科学院广州生物医药与健康研究院联合澳门大学,在《细胞研究》(Cell Research)上,在线发表了题为Rpd3S组蛋白去乙酰化酶复合物对核小体去乙酰化和DNA接头收紧的结构基础的研究论文。该研究通过生化手段和单颗粒冷冻电镜技术确定了Rpd3S组装模式,并以多种不同核小体底物模拟Rpd3S去乙酰化过程中的不同状态,捕获了Rpd3S在H3K36甲基化依赖的去乙酰化过程中的...
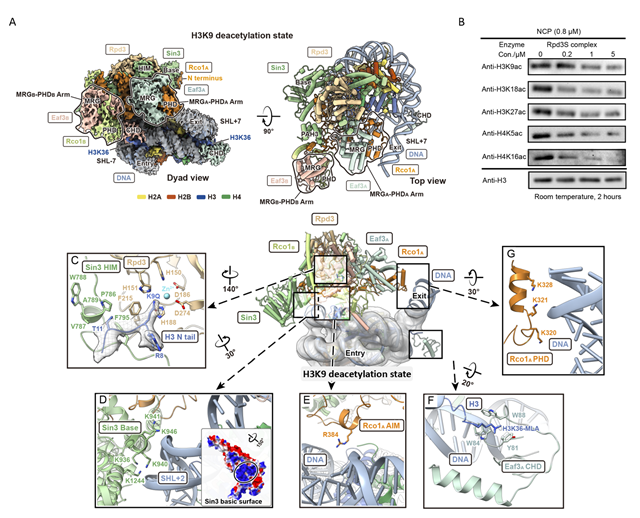
2023年9月5日,中国科学院广州生物医药与健康研究院与澳门大学合作在Cell Research在线发表题为Structural basis of nucleosome deacetylation and DNA linker tightening by Rpd3S histone deacetylase complex的研究论文。该研究通过生化手段及单颗粒冷冻电镜技术确定了Rpd3S组装模式,并...


在真核细胞分裂过程中,染色质结构的重新建立对于维持基因组完整性和表观遗传信息传递至关重要。DNA复制一方面破坏母链DNA的亲本核小体,另一方面新生核小体必须在DNA子链上重建。染色质组装因子CAF-1是在进化过程中保守的异源三聚体组蛋白伴侣复合物,负责将新合成的H3-H4组蛋白装配到子链DNA上,完成从头装配的核小体组装的第一步,即形成一个由DNA缠绕H3-H4四聚体组成的核小体组装中间态Tetr...


清华大学李海涛/闫创业合作揭示甲基化指引下的Rpd3S核小体去乙酰化动态调控模型(图)
表观遗传 清华大学 甲基化
2023/12/26
表观遗传是确保生物表型复杂性和多样性的关键机制。Rpd3是一类全局基因调控因子和共抑制因子,于1996年首次被报道作为组蛋白去乙酰化酶(HDAC)发挥作用;这一发现与同年组蛋白乙酰转移酶GCN5的转录共激活功能发现一起,标志了现代表观遗传学的兴起。作为Class-I类型HDAC的原型代表,来自酵母的Rpd3可以形成Rpd3S(分子量0.6兆道尔顿)和Rpd3L(分子量1.2兆道尔顿)两类多亚基酶分...

中国科学院生物物理研究所揭示PR-DUB去泛素化酶复合物特异性去除核小体H2AK119泛素化的分子机制(图)
PR-DUB 去泛素化酶 复合物特异性 核小体 H2AK119泛素化 分子机制
2023/4/7

中国科学院生物物理研究所许瑞明和朱冰课题组合作揭示PR-DUB去泛素化酶复合物特异性去除核小体H2AK119泛素化的分子机制(图)
PR-DUB 去泛素化酶 复合物特异性 核小体 H2AK119泛素化 分子机制
2023/4/25

2023年3月29日,中国科学院生物物理研究所研究员许瑞明与朱冰团队,在《自然》(Nature)上,在线发表了题为Basis of the H2AK119 specificity of the Polycomb repressive deubiquitinase的研究论文。该研究解析了人源PR-DUB复合物结合H2AK119泛素化核小体的高分辨率电镜结构,阐明了PR-DUB特异性去除核小体H2AK...

中国科学院深圳先进技术研究院等创造出含有定点共翻译修饰核小体的酵母菌(图)
定点共翻译 修饰核小体 酵母菌
2022/9/15

中国科学院深圳先进技术研究院创造含有定点共翻译修饰核小体的酵母菌(图)
核小体 酵母菌 蛋白赖氨酸
2023/8/8
随着蛋白质谱技术的发展,许多组蛋白赖氨酸残基的酰化修饰被鉴定出来,其中巴豆酰化修饰是一类在酵母、哺乳动物等真核生物中保守存在的组蛋白酰化修饰。自2011年被发现以来,巴豆酰化修饰俨然成为了领域内的研究热点。这是因为该修饰是一种重要的表观遗传机制调节基因转录的翻译后修饰。尽管巴豆酰化和乙酰化基团的化学结构类似,却可能存在不同于乙酰化修饰的生物学功能。因此,揭示不同酰化修饰在组蛋白同一位点的生物学功能...

核小体排布和染色质开放性是重要的表观遗传学信号,与基因表达调控,胚胎发育,组织分化等众多生理过程间存在紧密联系。目前,ATAC-seq因其对样品要求低,处理简单,可获得多维度染色质状态信息等优势成为表观遗传学的明星技术之一。然而在稀有样本或者单细胞样本中,ATAC-seq数据仍然相对稀疏。现有生物信息学技术在稀疏的ATAC-seq数据中普遍灵敏度不足。因此,研发能适用于低测序深度ATAC-seq文...
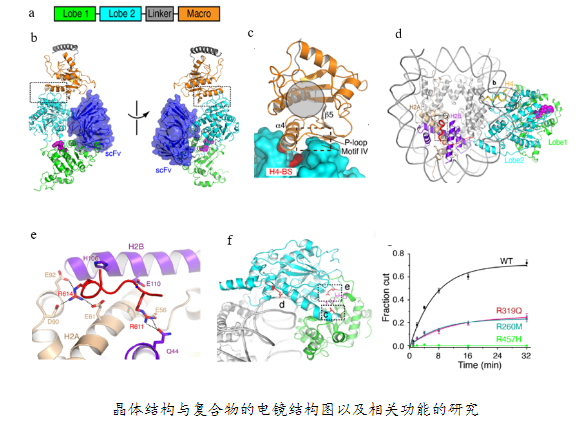
清华大学生命科学学院陈柱成教授课题组解析了染色质重塑蛋白ALC1自抑制状态下的晶体结构,以及ALC1-核小体复合物的冷冻电镜结构,结合相应的生化实验,揭示了ALC1是如何自抑制以及如何被核小体调控的机理。

北京师范大学生命科学学院王占新教授及其合作团队首次揭示了NSD家族组蛋白赖氨酸甲基转移酶修饰核小体的分子机理(图)
北京师范大学生命科学学院 王占新 NSD家族 蛋白 赖氨酸甲 分子机理 细胞生物学
2020/12/28
北京师范大学生命科学学院细胞生物学研究所王占新教授与国内外专家合作共同揭示了NSD家族蛋白催化核小体H3K36位点甲基化修饰的分子机理,该成果已于2020年12月24日在《Nature》上在线发表 (https://www.nature.com/articles/s41586-020-03069-8)。王占新教授和南方科技大学的冷冻电镜中心、美国斯隆凯特琳癌症研究所的Dinshaw Patel教授...
2020年12月24日,南方科技大学生物系高级研究学者李婉秋携手北京师范大学教授王占新团队、纪念斯隆-凯瑟琳癌症研究中心教授Dinshaw J. Patel团队和斯坦福大学教授Or Gozani团队在《自然》(Nature)杂志在线发表了题为“Molecular basis of nucleosomal H3K36 methylation by NSD methyltransferases(NSD...


