搜索结果: 1-15 共查到“药学 国家药监局”相关记录27条 . 查询时间(0.121 秒)
国家药监局 人力资源社会保障部关于印发执业药师继续教育暂行规定的通知
国家药监局 维吾尔自治区 新疆
2024/4/12
国家药监局 人力资源社会保障部关于印发执业药师继续教育暂行规定的通知
国家药监局:去年审评通过建议批准21个创新药,含3个首创新药
国家药监局 首创新药 中药提取物
2023/9/13
报告显示:全年审评通过建议批准21个创新药,含3个首创新药(First-in-Class);全年整体按审评时限审结率提升至99.80%;儿童用药批准数量为66个,创历史新高;10个中药新药(包含中药提取物)获批上市。
国家药监局关于修订《药品检查管理办法(试行)》部分条款有关事宜的通知
国家药监局关于发布《中药饮片标签管理规定》的公告(2023年第90号)
中药饮片 标签 管理规定
2023/8/4
为进一步规范中药饮片标签的管理,根据《中华人民共和国药品管理法》《中华人民共和国药品管理法实施条例》《药品说明书和标签管理规定》等法律、行政法规和规章,国家药监局组织制定了《中药饮片标签管理规定》,现予发布,自2024年8月1日起施行,其中,保质期的标注自2025年8月1日起施行。
国家药监局:解决药品说明书“看不清”问题
国家药监局 药品说明书 药品制剂
2024/2/3
记者从国家药监局获悉,国家药监局日前发布征求意见稿,决定在老年患者常用的部分口服、外用药品制剂中开展药品说明书适老化改革试点。
为优化药品说明书管理,解决药品说明书“看不清”等问题,鼓励药品上市许可持有人积极探索,国家药监局组织起草了《药品说明书适老化改革试点工作方案(征求意见稿)》以及《药品说明书(简化版)编写指南(征求意见稿)》《电子药品说明书(完整版)格式要求(征求意见稿)》。现向社会公开征求意见。
国家药监局综合司公开征求《药物临床试验机构监督检查办法(试行)(征求意见稿)》意见
人源性干细胞及其衍生细胞治疗产品在细胞来源、类型、制备工艺等方面异质性较大,治疗原理和体内活性作用相较传统药物更加复杂。为给该类产品开展临床试验提供技术指导和建议,在国家药品监督管理局的部署下,药审中心组织制定了《人源性干细胞及其衍生细胞治疗产品临床试验技术指导原则(试行)》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督...
国家药监局批准泽贝妥单抗注射液上市
国家药监局 泽贝妥 单抗注射液 安瑞昔
2023/8/4
近日,国家药品监督管理局批准浙江博锐生物制药有限公司申报的泽贝妥单抗注射液(商品名:安瑞昔)上市。该药品适用于CD20阳性弥漫大B细胞淋巴瘤,非特指性(DLBCL,NOS)成人患者,应与标准CHOP化疗(环磷酰胺、阿霉素、长春新碱、泼尼松)联合治疗。
国家药监局批准奥磷布韦片上市
国家药监局 奥磷布韦片 圣诺迪
2023/8/4
近日,国家药品监督管理局通过优先审评审批程序批准南京圣和药业股份有限公司申报的1类创新药奥磷布韦片(商品名:圣诺迪)上市。该药为我国自主研发并拥有自主知识产权的创新药,适用于与盐酸达拉他韦联用,治疗初治或干扰素经治的基因1、2、3、6型成人慢性丙型肝炎病毒(HCV)感染,可合并或不合并代偿性肝硬化。
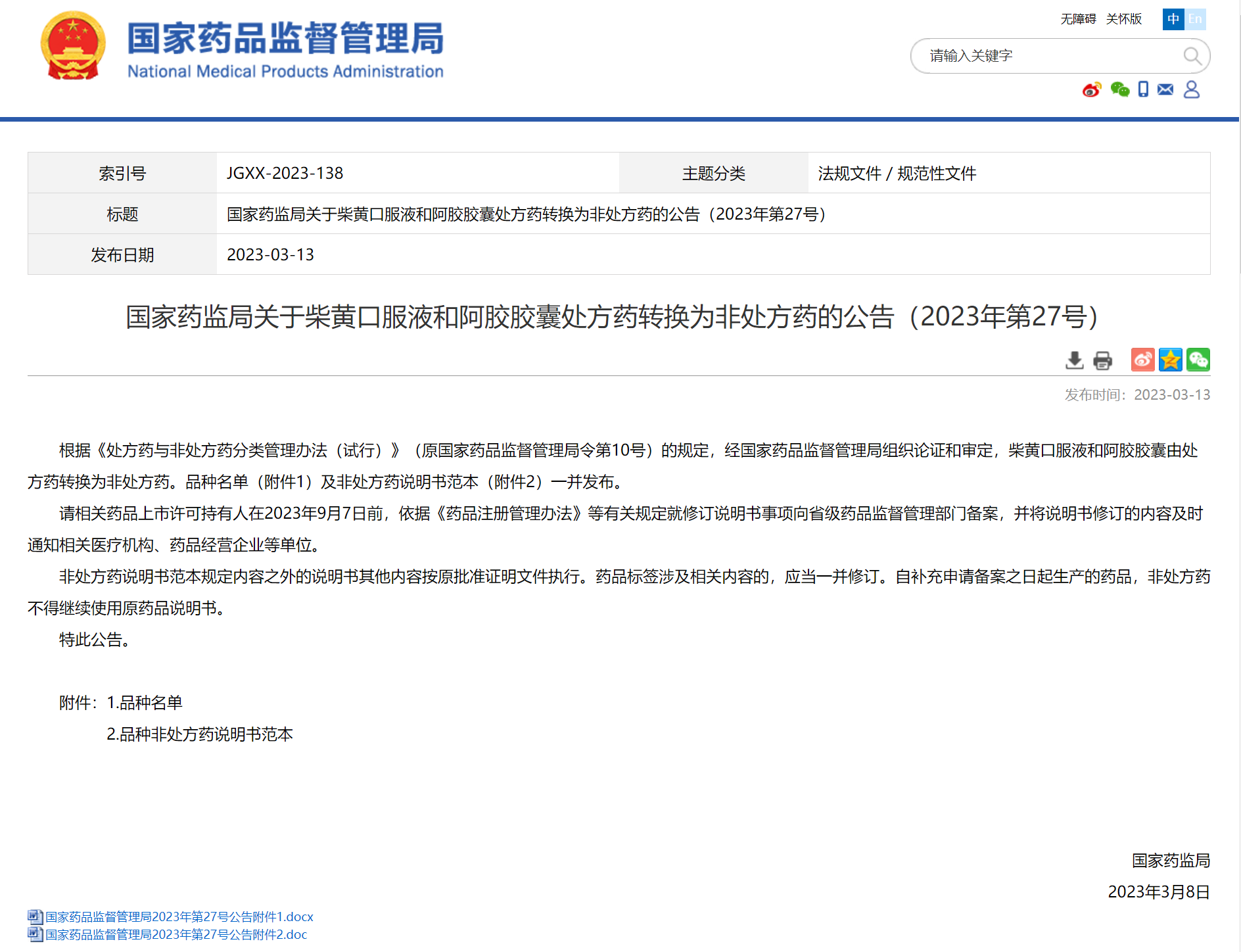
据国家药监局网站2023年3月13日消息,根据《处方药与非处方药分类管理办法(试行)》(原国家药品监督管理局令第10号)的规定,经国家药品监督管理局组织论证和审定,柴黄口服液和阿胶胶囊由处方药转换为非处方药。品种名单及非处方药说明书范本一并发布。

国家药监局批准13个新冠病毒感染对症治疗药物上市,均为口服剂型(图)
国家药监局 新冠病 口服剂 维生素C
2023/8/4
2023年1月3日,国家药监局通过快速审评通道,批准对乙酰氨基酚维生素C泡腾片等13个新冠病毒感染对症治疗药物上市。获批品种中9个品种为国家卫生健康委发布的《新冠病毒感染者居家治疗指南》中推荐的常用对症治疗药物,4个品种为医用氧。
为推动和规范我国放射性体内诊断药物的研发,在国家药品监督管理局的部署下,药审中心组织制定了《放射性体内诊断药物非临床研究技术指导原则》(见附件)。
中国首个用于治疗轻度哮喘的联合疗法获国家药监局批准
中国 轻度哮喘 联合疗法 国家药监局
2021/1/29
国家药品监督管理局日前正式批准了中国首个用于治疗轻度哮喘的联合疗法,用于成人和12岁以上青少年轻度哮喘患者的抗炎缓解治疗,并将为轻度、中度、重度哮喘患者提供全程管理方案。有研究显示,30%至40%的轻度哮喘患者可能发生严重的急性发作。为了有效控制症状并降低急性发作风险,轻度哮喘的早期抗炎干预非常重要。
国家卫生健康委、科技部、工业和信息化部、国家市场监管总局、国家药监局联合印发《疫苗生产车间生物安全通用要求》
国家卫生健康委 科技部 工业和信息化部 国家市场监管总局 国家药监局 疫苗生产车间 生物安全 通用要求
2020/6/19
国家卫生健康委、科技部、工业和信息化部、国家市场监管总局、国家药监局18日联合印发《疫苗生产车间生物安全通用要求》,作为新冠肺炎疫情防控期间推动新冠疫苗生产的临时性应急要求。利用病原微生物进行疫苗生产,具有一定的生物安全风险,需要在确保疫苗质量的同时,确保生产活动的生物安全。该文件参照国内外生物安全相关的法律法规和标准规范,紧密结合药品生产质量管理规范要求,基于疫苗生产全过程中的生物安全风险提出生...

